导电聚合物水凝胶(如:PEDOT:PSS水凝胶)因具优异的类生物组织柔性、导电特性和生物相容性等,广泛应用于生物电极涂层,构建力学/电学适配的交互界面,可用于各类生理紊乱和疾病的诊断、预警、以及后续治疗。然而,由于PEDOT:PSS水凝胶存在的本征脆性,在长期电学交互过程,这类水凝胶涂层极易发生疲劳破坏(如裂纹产生或涂层脱落),导致电极功能失效、生物组织损伤(如炎症产生或疤痕形成),极大地限制了它们在实际应用中的可靠性。因此,构建长期稳定高效的导电聚合物水凝胶电极涂层/界面,能有效解决现阶段生物电子领域存在的重大挑战,为新兴植入式生物电子的发展提供技术支持。
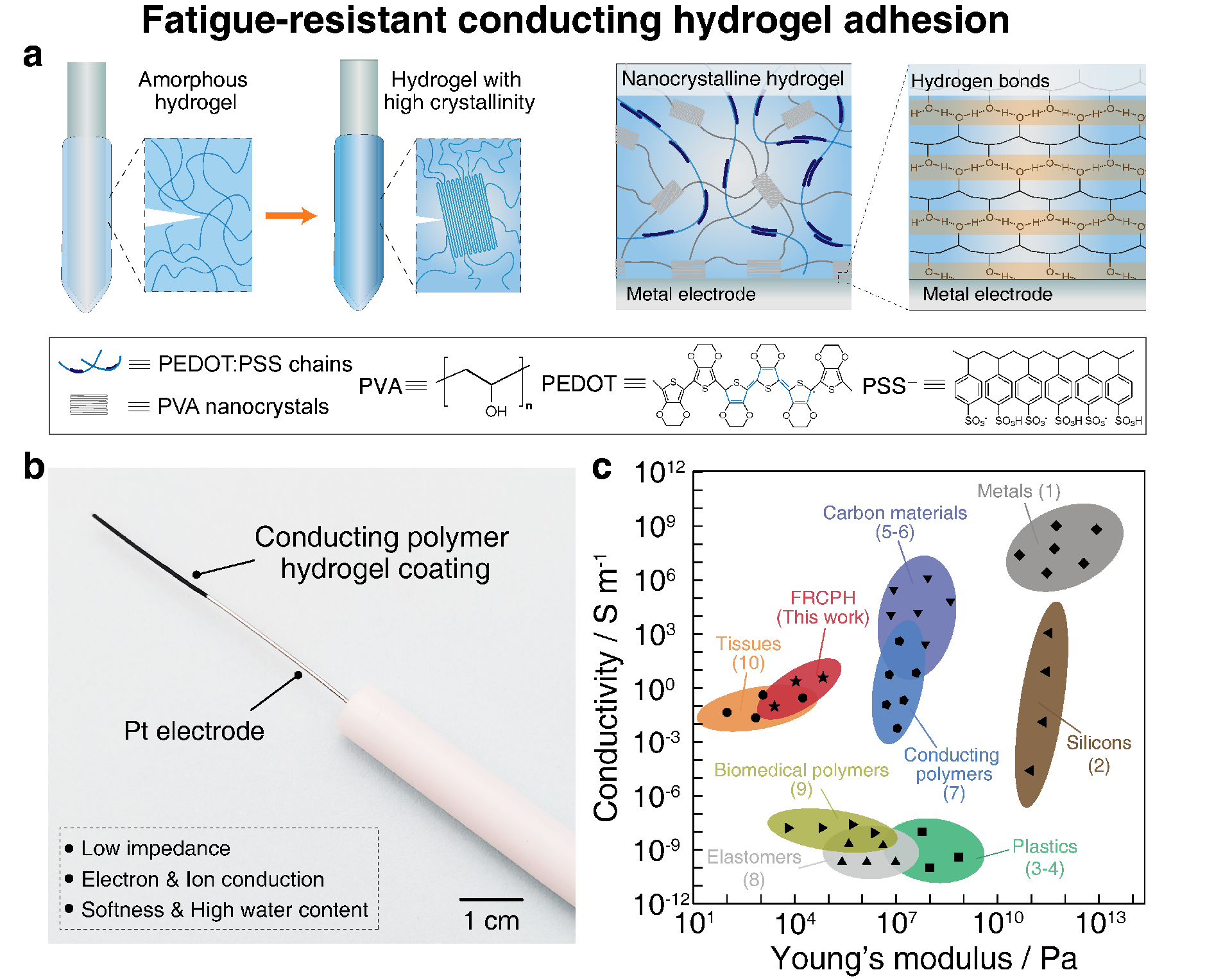
图1. 机械适应性水凝胶电极涂层的设计原理及性能比较。
该团队通过水凝胶-基底界面纳米晶域的有序调控,实现导电聚合物水凝胶与各类基底的抗疲劳粘合(图1),界面疲劳阈值由~2 J m-2提升到~330 J m-2(图2a-b)。这类水凝胶涂层能够提供与传统刚性电极截然相反的机械适应性界面、类生物组织的力学特性、以及离子/电子双导电模式,显著优于现阶段各类可植入电极和封装材料。此外,这种稳固的导电聚合类物水凝胶涂层展现出了优异的电化学稳定性,比如在超过10,000次循环伏安测试和1,000,000次双向电荷注入脉冲刺激后,水凝胶涂层仍然保持低阻抗、高电荷存储容量和注入能力(图2c),能够满足临床上对生物电子长期电化学稳定性的高要求。
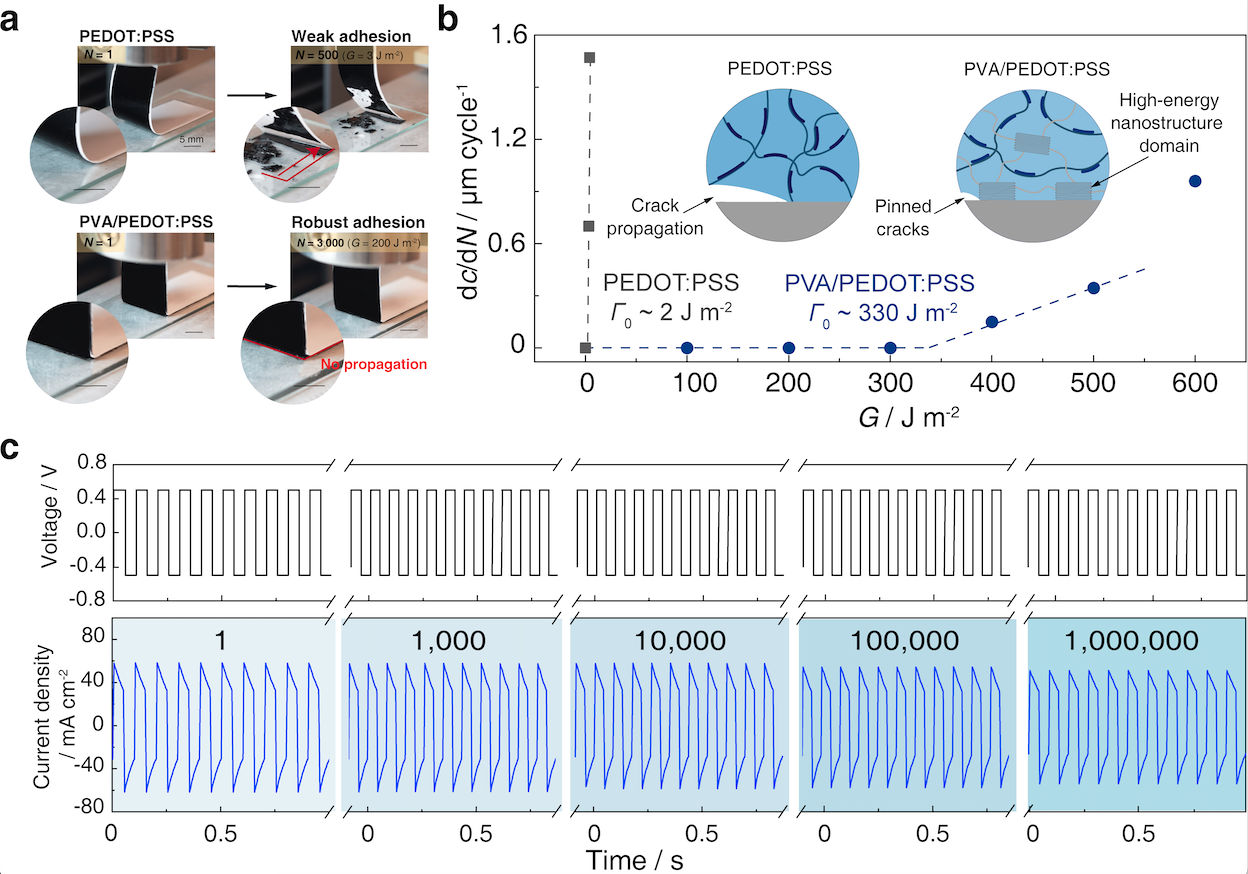
图2.导电聚合物水凝胶电极涂层的抗疲劳粘接和长期电化学稳定性。
该团队首先在Langendorff灌流的离体大鼠心脏上进行验证,使用这类稳固的导电聚合物类水凝胶涂层的优势:力学适应性界面和低界面阻抗能显著降低心脏起搏电压,能有效避免高电压刺激所引发的组织损伤等副作用;同时,高界面稳定性确保在数万次的电脉冲刺激过程后,水凝胶涂层仍可实现低电压低能耗的心脏起搏。
该团队进一步构建患病大鼠(窦性心律过缓)模型,验证了体内电刺激可以有效的调控心律过缓的症状(心率由病态的~140 bpm恢复到正常的~350 bpm),而且这类低电压电刺激不会造成任何组织损伤、炎症反应等生物安全性问题(图3)。同时,该团队结合体外长期老化实验和体内效果测试,证实了这类导电聚合物水凝胶涂层的机械和电化学稳定性,以及这类电极在体内疾病治疗调控上的潜力。
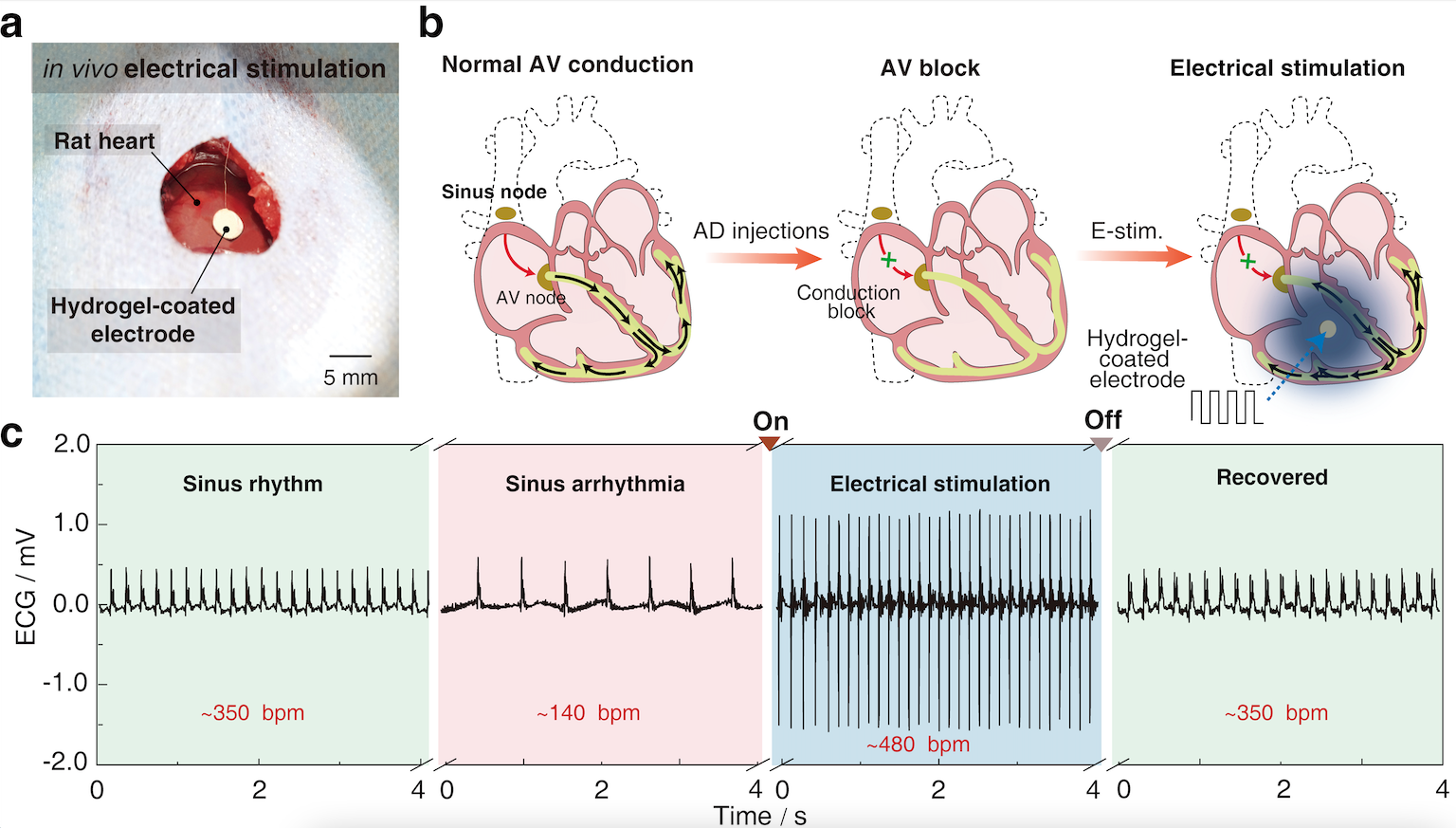
图3.在体内大鼠模型中使用导电聚合物水凝胶电极治疗AV阻滞。
南方科技大学博士生薛羽为文章的第一作者,刘吉副教授为通讯作者。该研究得到科技创新2030脑科学与类脑研究重大项目、深圳市政府和南方科技大学科研启动基金、深圳市科技创新委员会和广东省基础研究和应用基础研究等基金项目的资助。
论文链接:https://onlinelibrary.wiley.com/doi/epdf/10.1002/adma.202304095

 扫一扫加微信
扫一扫加微信